С тех пор как Селье обнаружил первые доказательства того, что стресс способен подавлять иммунитет, прошло почти 60 лет. Селье обнаружил,
_____________________________________________
¹ Как мы только что сказали, врожденная иммунная реакция основана на том, что в зараженную область проникают белки. Среди белков, которые борются с микробами, есть один, о котором мы говорили в главе 3, С-реактивный белок крови. Думаю, вы помните, что клейкие частицы, например холестерин, создают атеросклеротические бляшки только в тех местах, где повреждены кровеносные сосуды. Поэтому степень повреждения и сила воспаления кровеносных сосудов — хороший прогностический фактор риска атеросклероза. С-реактивный белок, как мы уже знаем, — самый надежный индикатор такого воспаления.
что у крыс, подвергавшихся воздействию различных неприятных факторов, могут атрофироваться иммунные ткани, например тимус. С тех пор ученые намного больше узнали об иммунной системе, и оказалось, что стресс нарушает очень многие иммунные функции.
Стресс подавляет формирование лимфоцитов, замедляет их циркуляцию в крови и сокращает время, в течение которого лимфоциты, уже находящиеся в крови, в ней остаются. Это угнетает производство новых антител в ответ на возбудителя инфекции и нарушает коммуникацию между лимфоцитами, уменьшая выработку соответствующих посредников. А это подавляет врожденную иммунную реакцию, поэтому воспаления не возникает. Так действуют самые разные стрессоры — физические и психологические, у приматов, крыс, птиц и даже рыб. И конечно, у человека.
Лучше всего такой процесс подавления иммунитета виден на примере глюкокортикоидов. Например, глюкокортикоиды могут вызывать уменьшение размеров тимуса; этот факт установлен вполне надежно. В былые времена (около 1960 года), когда мы еще не умели напрямую измерять количество глюкокортикоидов в крови, для этого использовали один косвенный способ: диагностику размеров тимуса. Чем меньше тимус, тем больше в крови глюкокортикоидов. Глюкокортикоиды угнетают формирование в тимусе новых лимфоцитов, а ведь ткань тимуса состоит преимущественно из этих новых клеток, готовых выйти в кровь. Глюкокортикоиды подавляют выработку посредников — интерлейкинов и интерферонов — и поэтому снижают чувствительность лимфоцитов к сигналу тревоги при возникновении инфекции.
Глюкокортикоиды, кроме того, вымывают лимфоциты из крови и заставляют их возвращаться в «хранилища» в иммунных тканях. Такое действие глюкокортикоидов угнетает в первую очередь Т-клетки, а не В-клетки. Это значит, что оно больше вредит клеточному иммунитету, а не иммунитету антител. И что самое интересное, глюкокортикоиды могут уничтожать лимфоциты. Это одна из самых горячих тем в медицине, получившая название запрограммированной гибели клеток¹. Клетки запрограммированы
_______________________________________________
¹ Еще один модный термин в этой области — апоптоз (от греческого ap o p to sis, означающего что-то вроде «отпадание», например «отпадание» осенью листьев на деревьях как их запрограммированная смерть). Ведутся большие споры о том, можно ли сказать, что апоптоз — это и есть запрограммированная гибель клеток, или он является только ее подтипом (я поддерживаю вторую гипотезу), а также, как ни странно, о том, нужно ли произносить в этом слове вторую «п» (я это делаю — мне нравится иной раз щегольнуть плебейским акцентом «человека с улицы»).
на то, чтобы иногда совершать самоубийство. Например, если клетка начинает превращаться в злокачественную, в ней активируется функция самоуничтожения, нейтрализующая ее до того, как она начнет процесс неконтролируемого деления; несколько типов раковых образований связаны с нарушением функции запрограммированной гибели клеток. Оказывается, что глюкокортикоиды с помощью нескольких механизмов способны запускать программу самоуничтожения у лимфоцитов.
Гормоны симпатической нервной системы, бета-эндорфин и КРГ в мозге также принимают участие в подавлении иммунитета во время стресса. В отличие от воздействия на иммунитет глюкокортикоидов механизмы такого влияния пока мало изучены. Эти гормоны традиционно считались менее важными, чем глюкокортикоиды. Однако множество экспериментов показывают, что стрессоры способны подавлять иммунитет независимо от секреции глюкокортикоидов с помощью других механизмов.
Почему иммунитет подавляется во время стресса?
Механизм, с помощью которого глюкокортикоиды и другие гормоны стресса подавляют иммунитет, — очень горячая тема современной цитобиологии и молекулярной биологии, особенно что касается уничтожения лимфоцитов. Но среди всех увлекательных открытий ультрасовременной науки было бы разумно задать вопрос о том, почему организм вообще допускает, чтобы его иммунная система была подавлена во время стресса. В первой главе я предложил одно объяснение; теперь, когда мы немного лучше представляем себе процесс стрессогенного подавления иммунитета, должно быть очевидно, что то мое объяснение не имеет никакого смысла. Я предположил, что во время стресса логично «закрыть» долгосрочные строительные проекты и направить энергию на более неотложные задачи — это касается и иммунной системы. Она прекрасно умеет находить опухоли, которые могли бы убить нас через шесть месяцев, или вырабатывать антитела, которые понадобятся нам через неделю, но не нужна в чрезвычайной ситуации, возникшей прямо сейчас.
Такое объяснение имеет смысл лишь в том случае, если стресс «заморозил » иммунную систему именно в том состоянии, в котором она находится сейчас, — больше никаких расходов на иммунитет, до тех пор пока чрезвычайная ситуация не закончится. Но на самом деле происходит иначе. Стресс приводит к большому расходу энергии, необходимой для демонтажа тканей иммунной системы — эти ткани съеживаются, их клетки разрушаются. Это нельзя объяснить простой «экономией» — ведь мы платим своей энергией за разрушение иммунной системы. И это приводит нас к теории, указывающей на более долгосрочные последствия этого процесса.
Почему эволюция позволила нам заниматься такими вопиющими глупостями? Уничтожать иммунную систему во время стресса! Возможно, для этого нет никаких серьезных причин. Но это не так глупо, как кажется. Не все функции организма можно объяснить с точки зрения эволюционной адаптивности. Возможно, стрессогенное подавление иммунитета — просто побочный продукт другой, вполне адаптивной функции; оно просто идет «в нагрузку».
Но вряд ли это так. Когда возникает инфекция, иммунная система вырабатывает химический посредник интерлейкин-1. Наряду с другими функциями он стимулирует гипоталамус к выработке КРГ. Как мы говорили в главе 2, КРГ стимулирует гипофиз, заставляя его вырабатывать АКТГ, который затем вызывает выработку глюкокортикоидов надпочечниками. Они, в свою очередь, подавляют иммунную систему. Другими словами, при некоторых обстоятельствах иммунная система побуждает организм вырабатывать гормоны, которые в итоге подавляют иммунную систему. Независимо от причин этого явления иммунная система иногда поощряет подавление иммунитета. Вероятно, это не случайно¹.
_________________________________________________
¹ Я тоже внес скромный вклад в эту науку: был участником группы, обнаружившей тот факт, что интерлейкин-1 стимулирует выработку КРГ. По крайней мере я так думал. Это было в середине 1980-х годов. Это была перспективная гипотеза, и лаборатория, где я работал, решила ее проверить благодаря моему предложению. Мы работали как маньяки, и однажды, в два часа ночи, я пережил тот момент эйфории, о котором мечтает любой ученый: я посмотрел на распечатку одной из машин, и меня осенило: «Ага, я был прав, вот как это работает: интерлейкин-1 высвобождает КРГ». Мы описали результаты, статья была принята престижным журналом Science, все были очень взволнованы, я позвонил родителям и т. д. Статью напечатали, но рядом с ней была опубликована работа об очень похожем исследовании группы швейцарских ученых, представленная в журнал на той же неделе. Это было по меньшей мере неприятно. (Возвращаясь к теме главы 2, если вы зрелый, уверенный в себе взрослый человек— каким я, к сожалению, бываю редко,— то способны получать удовольствие от подобных вещей: две лаборатории независимо друг от друга, с разных сторон земного шара, приходят к одинаковому выводу. Должно быть, мы действительно установили истину. Наука еще немного продвинулась вперед.)
В последние годы возникло множество гипотез в попытках объяснить, почему же во время стресса мы активно разрушаем собственный иммунитет при добровольном содействии самой иммунной системы. Некоторые из этих гипотез казались довольно вероятными, пока мы не узнали немного больше об иммунитете и не смогли их исключить. Другие были просто безумными, и даже я сам опрометчиво продвигал некоторые из них в первом издании этой книги. Но в последние 10 лет ответ был найден, и он перевернул все представления об этой сфере.
Сюрприз, сюрприз
Оказывается, что в первые несколько минут (скажем, около получаса) после начала действия стрессора мы не подавляем иммунитет как таковой — наоборот, мы улучшаем множество его аспектов (фаза А на приведенном ниже графике) (рис. 28). Это касается всех аспектов иммунитета, но прежде всего врожденного иммунитета. Это вполне логично — полезно активировать те аспекты иммунной системы, которые будут создавать для нас антитела в следующие несколько недель. Но еще полезнее немедленно активировать те элементы иммунной системы, которые могут выручить нас прямо сейчас. Чем больше иммунных клеток срочно отправляются в кровь, когда нервная система переживает травму, тем более сильное воспаление возникает в поврежденной ткани. Кроме того, циркулирующие в крови лимфоциты лучше вырабатывают иммунные посредники и лучше на них реагируют. И в слюну выделяется еще больше неспецифических антител врожденной иммунной системы. Такое повышение иммунитета происходит не только в ответ на инфекцию. Физические и психологические стрессоры, по-видимому, также запускают раннюю стадию активации иммунитета. Что еще интереснее, главные злодеи, подавляющие иммунитет, — глюкокортикоиды — играют в этом процессе важнейшую роль (вместе с симпатической нервной системой).
Итак, с началом действия любого стрессора наш а иммунная защита усиливается. Но если стресс продолжается долго, ситуация меняется на прямо противоположную. Примерно через час продолжающаяся активация глюкокортикоидов и симпатической системы начинает подавлять иммунитет. Если действие стрессора в это время заканчивается, что нам даст подавление иммунитета? Иммунная функции вернется в то состояние, с которого началась реакция, — назад к базовой линии (фаза В). Если сильные стрессоры действуют дольше или уровень глюкокортикоидов очень высокий, иммунная система не просто возвращается к базовой линии, а резко падает к тому уровню, где начинается подавление иммунитета (фаза С). Для большинства аспектов иммунной системы, которые можно измерить, длительное действие сильных стрессоров снижает показатели на 40-70% ниже базовой линии.
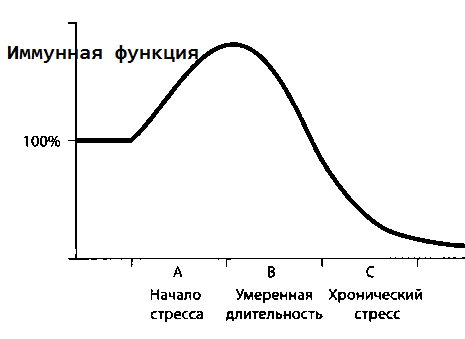
Гипотеза о временной активации иммунной системы в начале действия стрессора вполне логична (по крайней мере не меньше, чем некоторые замысловатые теории о том, почему имеет смысл подавление иммунитета). Как и идея о том, что все, что повышается, должно в итоге снизиться. И, как мы часто видим на страницах этой книги, если у нас есть стрессор, который действует слишком долго, адаптивное снижение к базовой линии может зайти слишком далеко. И тогда мы попадаем в беду.
Почему нам потребовалось так много времени, чтобы это выяснить? Вероятно, по двум причинам. Во-первых, потому что многие методы измерения различных показателей иммунной системы только недавно стали достаточно чувствительными, чтобы отмечать небольшие, быстрые различия. Раньше ученым не удавалось «поймать» фазу А, эту быструю вспышку стимуляции иммунной системы в начале действия стрессора. Поэтому в течение многих десятилетий мы думали, что изучаем иммунную реакцию на стресс, а на самом деле изучали восстановление иммунной реакции на стресс. Во-вторых, в этой области ученые обычно исследуют действие сильных, длительных стрессоров или влияние большого количества глюкокортикоидов в течение длительных периодов. Это создает определенный перекос в планировании и проведении экспериментов — они обычно предполагают сильное воздействие. Если при этом ничего не происходит, выбирается новая область исследований. А если что-то происходит, повторяется достаточно много раз и вы уверены, что это происходит, только после этого можно начинать думать о более тонких нюансах. Поэтому в начале исследований в этой сфере ученые изучали только те стрессоры или паттерны воздействия глюкокортикоидов, которые переводят организм в фазу С, и только позже пришло время для изучения более тонких аспектов, возникающих на фазе В.
Это произошло благодаря экспериментам Аллана Мунка из Дартмутского университета, одного из крестных отцов данной области, еще в середине 1980-х предсказавшего почти все недавние открытия. Он также предсказал ответ на другой важный вопрос. Зачем возвращать иммунную функцию к дострессовому уровню (фаза В на диаграмме)? Почему просто не оставить ее на более активированном, более высоком уровне, достигнутом в первые 30 минут, и не воспользоваться этой активацией на следующих фазах? Выражаясь метафорически, почему бы и дальше не держать армию в состоянии максимальной мобилизации? Прежде всего, это очень дорого. Что еще важнее, система, постоянно находящаяся в состоянии максимальной готовности, в какой-то момент не выдержит, и в результате «дружественного огня» может пострадать кто-то из «своих». Так может случиться и с иммунной системой, если она хронически активирована: она начинает путать с агрессором части собственного организма. Так возникают аутоиммунные заболевания.
Такие рассуждения привели Мунка к гипотезе о том, что если вы не прошли фазу В и не вернули активированную иммунную систему к базовой линии, то у вас растет риск аутоиммунных заболеваний. Эта идея была подтверждена по крайней мере в трех областях. Во-первых, можно искусственно заблокировать у крыс уровень глюкокортикоидов в низком базовом диапазоне, а затем подвергнуть их стрессу. При этом у животных возникнет фаза А (по большей части под воздействием адреналина), но не будет расти уровень глюкокортикоидов, и это не позволит им полностью перейти в фазу В. При этом у крыс возрастет риск аутоиммунных заболеваний. Во-вторых, врачам иногда приходится удалять пациенту один из двух надпочечников (источник глюкокортикоидов), как правило, из-за опухоли.
Сразу же после этого уровень глюкокортикоидов в крови падает вдвое и остается таким до тех пор, пока оставшийся надпочечник не начнет вырабатывать их вдвое больше. В период низкого уровня глюкокортикоидов у пациентов чаще возникают симптомы аутоиммунных или воспалительных заболеваний — в организме недостаточно глюкокортикоидов, чтобы перейти в фазу В, когда возникает какой-то стресс (рис. 29). Наконец, если исследовать популяцию крыс или, как ни странно, цыплят, у которых спонтанно возникают аутоиммунные заболевания, у них отмечаются нарушения глюкокортикоидной системы — или уровень этого гормона слишком низкий, или иммунные клетки нечувствительны к глюкокортикоидам. То же самое касается людей, страдающих аутоиммунными заболеваниями, например ревматоидным артритом.
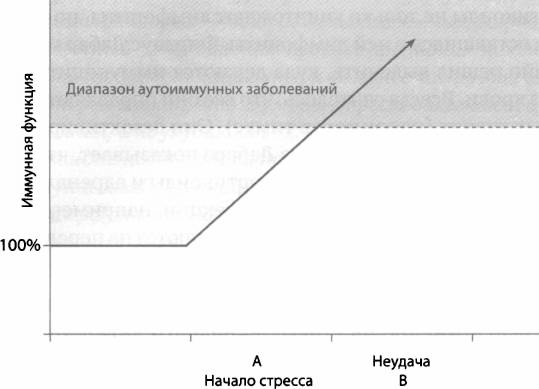
Таким образом, в начале реакции на стресс иммунная система активируется, а не подавляется. Оказывается, благодаря реакции на стресс активация иммунной функции не перерастет в аутоиммунный процесс.
Это открытие привело к некоторому пересмотру представлений в данной области. Если стресс продолжается достаточно долго и начинает подавлять иммунитет, некоторые элементы, традиционно считавшиеся свидетельством подавления иммунитета, на самом деле оказались признаками его укрепления.
Это проявляется двумя способами. Если кто-то принимает большую дозу глюкокортикоидов или в течение многих часов подвергается действию очень мощного стрессора, то его гормоны начнут уничтожать лимфоциты без разбора, просто убивать их. Если ненамного повысить уровень глюкокортикоидов (так происходит в начале фазы В), то гормоны будут уничтожать только определенную подгруппу более старых лимфоцитов, которые и так неэффективны. На этом этапе глюкокортикоиды помогают укреплять иммунную реакцию, избавляясь от лимфоцитов, бесполезных в текущей чрезвычайной ситуации. Это является косвенным подтверждением укрепления иммунной функции.
Вторая тонкость отражает новую интерпретацию того, что люди знали испокон веков (по крайней мере во времена Селье). Как мы уже знаем, глюкокортикоиды не только уничтожают лимфоциты, но и вытесняют из крови еще оставшиеся в ней лимфоциты. Фирдаус Дабар из Университета штата Огайо решил выяснить, куда деваются иммуноциты, которые вытеснены из крови. Всегда считалось, что все они оправляются в хранилища в иммунных тканях (например, в тимус). Они дезактивируются, и от них уже нет никакой пользы. Но работа Дабара показывает, что не все они отправляются на консервацию. Глюкокортикоиды и адреналин отправляют многие из этих лимфоцитов к месту инфекции, например в кожу. То есть иммуноциты не дезактивируются, а отправляются на передовую. Поэтому, например, царапины на коже заживают быстрее.
Таким образом, в начале действия стрессора глюкокортикоиды и другие гормоны, реагирующие на стресс, ненадолго активируют иммунную систему, улучшая иммунную защиту, оттачивая ее, доставляя иммунные клетки к месту битвы с инфекцией. Но если действие глюкокортикоидов продолжается, система может промахнуться и войти в аутоиммунное состояние. Поэтому при длительном стрессе возникает обратный эффект: система возвращается к базовой линии. Во время патологического сценария, когда на организм действуют сильные и длительные стрессоры, иммунитет падает ниже базовой линии.
Эти новые открытия помогают объяснить один из самых упрямых парадоксов в этой области. Он касается аутоиммунных заболеваний. Вот два факта об аутоиммунных процессах:
1. Поскольку аутоиммунные заболевания связаны с избыточной активацией иммунной системы (до такой степени, что здоровые функции и органы тела она начинает воспринимать как агрессора), самое распространенное и освященное веками лечение таких болезней состояло в том, чтобы посадить пациента «на стероиды», давая ему большие дозы глюкокортикоидов. Логика здесь очевидна: это резко подавляет иммунную систему и она больше не может нападать на поджелудочную железу, нервную систему или на какой-то другой объект своего неуместного рвения (и, как очевидный побочный эффект этого подхода, иммунная система также будет не слишком эффективно защищать пациента от реальных патогенов). Поэтому назначение больших доз гормонов стресса облегчает симптомы аутоиммунных болезней. Кроме того, выяснилось, что длительное действие сильных стрессоров снижает симптомы аутоиммунных заболеваний у лабораторных крыс.
2. В то же время, по-видимому, стресс может усугублять аутоиммунные заболевания. Стресс— один из самых надежных факторов (если не самый надежный), ухудшающих прогноз при таких заболеваниях. Об этом часто сообщают пациенты, и не менее часто это игнорируют врачи, которые знают, что гормоны стресса облегчают аутоиммунные состояния, а не ухудшают их. Но некоторые объективные исследования также подтверждают эту гипотезу, например для таких аутоиммунных заболеваний, как рассеянный склероз, ревматоидный артрит, диффузный токсический зоб, язвенный колит, воспалительные заболевания кишечника и бронхиальная астма. Сейчас есть всего несколько таких отчетов, и многие им не доверяют, потому что они основаны на ретроспективных данных, взятых из самоотчетов пациентов, а не на научных экспериментах. Однако результаты довольно однородны: у многих больных дебют аутоиммунных заболеваний, и в еще большей степени их периодические обострения, коррелирует со стрессом. Кроме того, к настоящему времени уже есть довольно обширная литература, подтверждающая, что стресс может ухудшать симптомы аутоиммунных заболеваний у животных.
Так как же действуют глюкокортикоиды и стресс — они ухудшают или облегчают симптомы аутоиммунных заболеваний? Приведенный ниже график дает ответ, который не удавалось найти раньше. Мы обнаружили два сценария, которые увеличивают риск аутоиммунных заболеваний. Во-первых, кажется, что многочисленные кратковременные стрессоры (то есть многократное прохождение фаз А и В) увеличивают риск аутоиммунных процессов. Почему-то повторяющиеся подъемы и спады ведут систему вверх, повышая вероятность аутоиммунных заболеваний. Во-вторых, не очень полезно, когда много раз за фазой А идет фаза В, но если за фазой А не возникает фаза В, это также увеличивает риск аутоиммунного процесса. Если нет адекватной фазы В, начинает раскручиваться спираль иммунной системы и возникает аутоиммунный процесс (рис. 30).
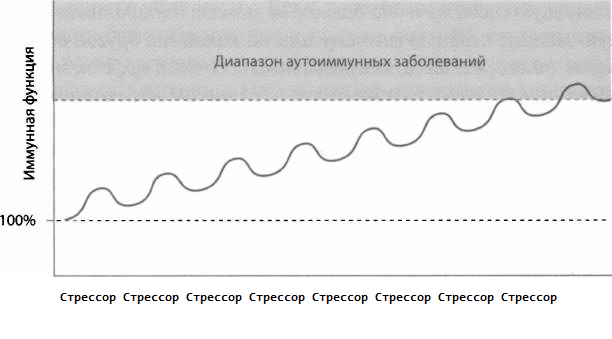
Как и следовало ожидать, если вместо этого мы имеем сильные и длительные стрессоры или вводим в организм большие дозы глюкокортикоидов, то система перейдет в фазу С — возникнет мощное подавление иммунной функции, уменьшающее аутоиммунные симптомы. Эту гипотезу поддерживает еще одно открытие: острый стресс увеличивает у крыс риск рассеянного склероза, а хронический стресс подавляет симптомы этого аутоиммунного заболевания. Очевидно, в процессе эволюции система не была предназначена для того, чтобы иметь дело с многочисленными повторными «включениями/выключениями», и поэтому возникает нарушение координации, увеличивая риск аутоиммунных процессов в системе.
Предыдущая – Глава 8. Иммунитет, стресс и болезни | Следующая – Хронический стресс и риск заболеваний





.jpg)
.jpg)
.jpg)
















